D लहंगा उठावल पड़ी महंगा Lahunga Uthaw 1
विशाल समाचार, डी-फ्रेंड्स: एफ़रेज़ा के रूप में जाना जाने वाला नया तेज़ अभिनय इनहेलेटबल इंसुलिन ने अभी तक एफडीए अनुमोदन प्राप्त किया है!
तीसरे समय में इनहेलबल इंसुलिन के इस नए फॉर्मूलेशन के लिए आकर्षण, दूसरी बार यह यू एस एस के नियामक प्रक्रिया के माध्यम से बनाने के बाद फाइजर की असफल एक्सबाबेर एक दशक पहले का बेहतर हिस्सा था।
शुक्रवार को, कैलिफोर्निया बायोटेक कंपनी मन्निकिंद कार्पोरेशन ने आखिरकार अपने अफ्रेजा डिवाइस के लिए नियामक निकासी प्राप्त की।

अब, अक्तूबर 2013 में अफरेज़ा को फिर से भेजने के बाद, मानकिंड ने आखिरकार एफडीए को आश्वस्त किया है कि वह मधुमेह के साथ वयस्कों के हाथों में प्रवेश करने के लिए तैयार है!
हम मानकिंड के शीर्ष अधिकारियों द्वारा बताए गए हैं कि वे अफरेज़जा के निर्माण और वितरित करने के लिए एक फार्मा पार्टनर खोजने के लिए काम कर रहे हैं, और यह उत्पाद जनवरी, या 2015 की पहली तिमाही के अंत तक उपलब्ध कराया जा सकता है। > शुक्रवार को जारी एफडीए समाचार रिलीज में, एजेंसी के डिवीजन ऑफ मेटाबोलिज़्म एंड एंडोक्रिनोलॉजी प्रोडक्ट्स के डॉ। जीन-मार्क गेट्टियर कहते हैं: "आज की मंजूरी मधुमेह के समग्र प्रबंधन में रात का समय इंसुलिन देने के लिए उपलब्ध विकल्पों को विस्तृत करती है, जो इसे आवश्यकता होती है रक्त शर्करा के स्तर को नियंत्रित करने के लिए। "
अफरेज़ा एक अल्ट्रापरैप-अभिनय इंसुलिन है जो पाउडर के रूप में तैयार किया गया है जिसे वयस्कों के लिए पूर्व-भोजन इंसुलिन के रूप में बनाया गया है (अभी तक बच्चों के लिए नहीं ) प्रकार 1 या टाइप 2 मधुमेह के साथ इसका उद्देश्य भोजन के बाद रक्त शर्करा के स्पाइक्स है, जिसका मतलब है कि मौजूदा इंसुलिन उपचार के साथ प्रयोग किया जाता है और इसका मतलब अकेले इंसुलिन उपचार नहीं है।
पाउडर इंसुलिन एक सीटी-आकार वाले इनहेलर के माध्यम से ड्रीमबोट नामक माध्यम से प्रशासित किया जाता है, जिसे पहले एफडीए दौर के बाद विकसित किया गया था और देरी का कारण था क्योंकि एजेंसी उस नए इनहेलर का उपयोग करने के लिए अधिक नैदानिक अध्ययन चाहते थे। फेफड़ों में डालने के तुरंत बाद पाउडर घुल जाता है, और इंसुलिन का काम शुरू करने के लिए जल्दी से खून में फेंक दिया जाता है। अफ़रेज़ा 12 से 15 मिनट के भीतर चोटियों और एक घंटे के भीतर प्रणाली से बाहर है, वर्तमान अल्पावधि इंसुलिनों की तुलना में आमतौर पर कम से कम 20 मिनट लगते हैं, 2-3 घंटे में चोटी, और सिस्टम में रह सकते हैं लंबे समय तक पांच घंटे।
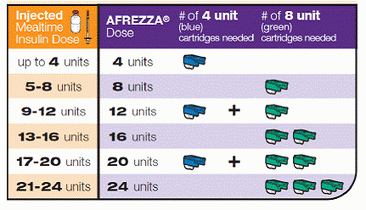
यह कैसे आप इसके लिए खुराक कर सकते हैं, वर्तमान इन्सुलिन इंजेक्शन या बोल्ट की मात्रा को अफ़्रीज़ा के अनुकूल अस्थिर खुराक में परिवर्तित कर सकते हैं:
व्यक्तिगत रूप से, यह मुझे खाने से कुछ खाने के लिए बहुत सारे इंसुलिन की तरह नहीं लगता उच्च खुराक की आवश्यकता होती है … मैं उन छोटी कारतूसों की एक पूरी गुच्छा के माध्यम से जा रहा था तो कुछ पीडब्लूडी के लिए, यह डिवाइस आसानी से हम की मात्रा को खोदने के मामले में एक लॉजिस्टिक चुनौती प्रस्तुत कर सकता है …? लेकिन फिर से, यह सुधार खुराक के साथ जिद्दी उच्च रक्त शर्करा नीचे दस्तक के लिए यह एक अच्छा उपकरण हो सकता है।
शुक्रवार देर से एक फोन पर बातचीत में, MankKind के अध्यक्ष Hakan Edstrom हमें बताया कि कंपनी ने अभी तक निर्माता और निर्माता के लिए संभावित भागीदारों के साथ किसी भी सौदे को अंतिम रूप नहीं दिया है Afrezza वितरित लेकिन यह करीब हो रही है, और जितनी जल्दी हो सके एक साझेदारी को अंतिम रूप देने के लिए कई कंपनियों के साथ बातचीत कर रही है।
लागत टीबीडी (बहुत कुछ संभावित साझेदारी पर निर्भर करता है) बनी हुई है, लेकिन एडस्ट्रॉम का कहना है कि वे कीमतें उसी सीमा में होने की उम्मीद करते हैं क्योंकि हम मरीज़ों को अमरीका में इंसुलिन पेन के लिए अब कितने भुगतान करते हैं
यह अनुमोदन एक विशाल विकास है, और यह लंबे समय से आ रहा है, आठ साल बाद यह खोज अल्फ्रेड मान द्वारा शुरू हुई - जिसने कम से कम मिनट की स्थापना की थी, अंततः मैदट्रोनिक द्वारा खरीदा गया था। हम साल के लिए अफरेज़ा की कहानी का पालन कर रहे हैं। 'मेरा
- प्रारंभिक एफडीए फाइलिंग दिनों से जब मैनकिंड का प्रारंभिक क्लैकरियर डिज़ाइन था, हालिया कवरेज के लिए कि कैसे आफ़्रीज़ा का उपयोग कृत्रिम अग्नाशय में क्लिनिकल परीक्षण।
सभी ने कहा, यह अभी भी एक आश्चर्य की बात है कि एजेंसी के स्वयं के कर्मचारियों की समीक्षा में एफआरए के अनुमोदन के कारण अफरेज़ा को उत्पाद की सुरक्षा और प्रभावशीलता के बारे में अनुमान लगाया गया था। प्रारंभिक चिंताएं थीं कि फेफड़ों के इंसुलिन के दीर्घकालिक संपर्क में फेफड़ों के कैंसर का कारण हो सकता है, क्योंकि नैदानिक परीक्षण के आंकड़ों में फैरस के कैंसर के अधिक मामले सामने आए थे, जो नियंत्रण समूहों में दूसरों की तुलना में अफरेज़ा प्राप्त करते थे। लेकिन संख्याएं छोटी थीं और निश्चित रूप से दूर थीं, और मानकिंड को उस जोखिम का आकलन करने के लिए दीर्घकालिक अध्ययन करने की आवश्यकता थी।
इस साल की 1 अप्रैल को हुई सलाहकार समिति ने 13 से 1 के बीच मतदान किया कि अफरेज़ा टाइप 1 मधुमेह के लिए इलाज के रूप में स्वीकार्य के लिए सुरक्षित और प्रभावी था, अकेले असंतोष वाले डेविड कुके ने मतदान करते हुए कहा कि जोखिम के प्रकार 1s।उन्होंने आंतरिक एफडीए की समीक्षा की ओर इशारा किया कि कुछ रोगियों ने अफरेज़ो को लेने से ब्रोन्कियल ऐंठन, खाँसी और उनके फेफड़ों के कामकाज में गिरावट के बाद उपचार बंद कर दिया। लेकिन उन चिंताओं में से कोई भी नहीं था, जिसे एफ़रेज़ा पर 2 प्रकार के उपयोग के लिए मतदान के दौरान आया, और समिति ने 14-0 वोट के साथ सर्वसम्मति से निर्णय लिया।अफ्रज़ा को अनुमोदन करने में, एफडीए ने कई सुरक्षा, प्रभावशीलता और रोगी उपयोग की शर्तों को संलग्न किया है:

अफ़्रीज़ा को वयस्कों के लिए ही मंजूरी मिलती है, न कि बच्चों के लिए। हालांकि, एजेंसी ने बाल चिकित्सा रोगियों में सुरक्षा और उपयोग का मूल्यांकन करने के लिए एक पोस्ट-मार्केट नैदानिक परीक्षण के लिए कहा है।
एफडीए को एक बॉक्सिंग चेतावनी की आवश्यकता है, सलाह देनी चाहिए कि अस्थमा और पुराने अवरोधक फुफ्फुसीय बीमारी (सीओपीडी) वाले कुछ लोगों ने अफरेज़ा का उपयोग किया है जो तीव्र ब्रोन्कोस्पास्सम का अनुभव किया है। नतीजतन, पुरानी फेफड़े की बीमारी, अस्थमा या सीओपीडी वाले लोगों को इस जोखिम के कारण अफरेज़ा का उपयोग नहीं करना चाहिए। चिकित्सीय परीक्षणों में अफरेज़ा के साथ जुड़े सबसे आम प्रतिकूल प्रतिक्रियाएं हाइपोग्लाइसीमिया, खांसी, और गले के दर्द या जलन थे।
- अनुमोदन आवश्यकताओं का एक हिस्सा जोखिम मूल्यांकन और निवारण रणनीति है, जिसमें अफरेज़ा के साथ जुड़े तीव्र ब्रोन्स्पॉस्जम के गंभीर खतरे के बारे में स्वास्थ्य देखभाल पेशेवरों को सूचित करने के लिए संचार योजना शामिल करनी होगी। इसका मतलब यह सुनिश्चित करने के लिए है कि लाभ अफरेज़ा के उपयोग के संभावित जोखिमों से अधिक है।
- अन्य पोस्ट-मार्केट स्टडीज़ को अफरेज़ा पर जरूरी है, जैसे कि: फुफ्फुसीय दुर्दमता के संभावित जोखिम का मूल्यांकन करने के लिए क्लिनिकल परीक्षण (यह मुक़ाबला भी कार्डियोवस्कुलर जोखिम और एफ़रेज़ो के पल्मोनरी फ़ंक्शन पर दीर्घकालिक प्रभाव का मूल्यांकन करेगा); और दो फार्माकोकाइनेटिक-फार्माकोडायनेमिक एउगसेकेमिक ग्लूकोज क्लैंप नैदानिक परीक्षण, एक को खुराक प्रतिक्रिया को चिह्नित करने और एक व्यक्ति को भीतर-विषय परिवर्तनशीलता को चिह्नित करने के लिए।
- एडस्ट्रॉम ने हमें बताया कि वे जल्द से जल्द बाल चिकित्सा परीक्षण शुरू करने की योजना बना रहे हैं, जो वास्तविक 2015 के मध्य में कुछ समय से शुरू होगा। इसका अर्थ है कि अफेज़्ज़ा को 2017 तक मधुमेह वाले बच्चों के लिए अनुमोदित नहीं किया जा सकता है, और उस नियामक प्रक्रिया में इस बात के आधार पर भिन्न हो सकते हैं कि बाजार के बाद के अध्ययन और प्रौढ़-उपयोग के अनुभव के बीच में क्या पता चलता है।
- और एफडीए के हरे रंग के प्रकाश के बावजूद, कोई गारंटी नहीं है कि अफरेज़ को वाणिज्यिक सफलता मिलेगी या पीडब्लूडी इसका उपयोग करने के लिए झुंड जाएगी। जैसा कि उल्लेख किया गया है, मन्निकंद ने अभी तक किसी भी फार्मा सहयोगी को अफरेज़ा को बेचने के लिए तैयार नहीं किया है। लेकिन अगर मन्निकुद्दी की मई में आय की कमाई जल्द ही आ रही है, तो इसका कोई संकेत नहीं हो सकता है, संभावित भागीदारी अभी दूर नहीं हो सकती।
- निवेशक के नजरिए से, कई लोग असफल प्रेज़बेरा इन्हेल्सन पर आधारित उलझन में हैं जिन्होंने पिछले कई वर्षों से अफरेज़ा के बारे में ज्यादा चर्चा की है। उस संयुक्त फाइज़र-सोनोफी उत्पाद को 2007 में एक साल से अधिक की बिक्री के बाद बाजार में खींच लिया गया था - जिसके परिणामस्वरूप रिकार्ड तोड़ने वाला $ 2 था। विक्रेताओं के लिए 8 बिलियन नुकसान
बेशक, मन्निकंद का दावा है कि अफरेज़ा काफी अलग है, मुख्यतः क्योंकि एक्सबुरा ने एक चक्करदार पैर-लंबे इनहेलर का इस्तेमाल किया था और फाइजर के नतीजे को दूर नहीं किया जा सकता था।
हम देखेंगे कि डी-कम्यूनिटी अब अफरेज़ा के साथ क्या सोचता है, खासकर सभी एपी नैदानिक परीक्षणों के साथ यह हाल ही में हुआ था। चाहे जनता को समझाने के लिए पर्याप्त है … अभी तक अस्पष्ट नहीं है …
अब के लिए खबर लेना, और हम देखेंगे कि यह हमारे लिए कितना लंबा समय लगता है और इस उत्तेजना को वास्तविक बिक्री और व्यापक उपयोग में बदल देता है।
अस्वीकरण
: मधुमेह खान टीम द्वारा बनाई गई सामग्री ज्यादा जानकारी के लिए यहां क्लिक करें।
अस्वीकरण
यह सामग्री मधुमेह के लिए बनाई गई है, एक उपभोक्ता स्वास्थ्य ब्लॉग मधुमेह समुदाय पर केंद्रित है। सामग्री की मेडिकल समीक्षा नहीं की गई है और हेल्थलाइन के संपादकीय दिशानिर्देशों का पालन नहीं करता है। मधुमेह खान के साथ स्वास्थ्य की साझेदारी के बारे में अधिक जानकारी के लिए, कृपया यहां क्लिक करें।अफरेज़ा इनहेल्ड इंसुलिन के लिए हमारी सांस पकड़े हुए

मधुमेहमाइन यह देखता है कि नया अफ्रज़ा इंहेल इंसुलिन उत्पाद बाजार के रास्ते में कैसे है, और यह क्या है मधुमेह प्रबंधन के भविष्य के लिए इसका मतलब है
साँस इंसुलिन अफरेज़ा को एफडीए अनुमोदन दिया गया है

एफडीए ने एक नया साँस इंसुलिन उत्पाद को मंजूरी दी है। Afrezza पाउडर के रूप में एक अल्ट्रारापिड-अभिनय इंसुलिन है, जिसे टाइप 1 मधुमेह के लिए पूर्व भोजन के रूप में बनाया गया है।
साँस इंसुलिन और अफरेज़ा: आपको क्या चाहिए

मधुमेहमैं मधुमेह के लिए इनहेलेटबल इंसुलिन का इतिहास बताता है, अफरेज़ा की स्थिति और अधिक।


